研究方向
基于机器学习和人工智能的成药性和安全性预测方法研究
不良的药代动力学性质(吸收、分布、代谢和排泄,ADME)和毒性(T)是导致药物开发失败的主要原因之一,因此在药物研究的早期阶段对候选药物分子的ADMET性质进行评估是至关重要的。目前ADMET评价的难点在于高质量成药性数据的缺乏和关键性ADMET指标高精度预测模型的构建。我们课题组发展了数据→模型→程序一体化的成药性预测理论研究体系。
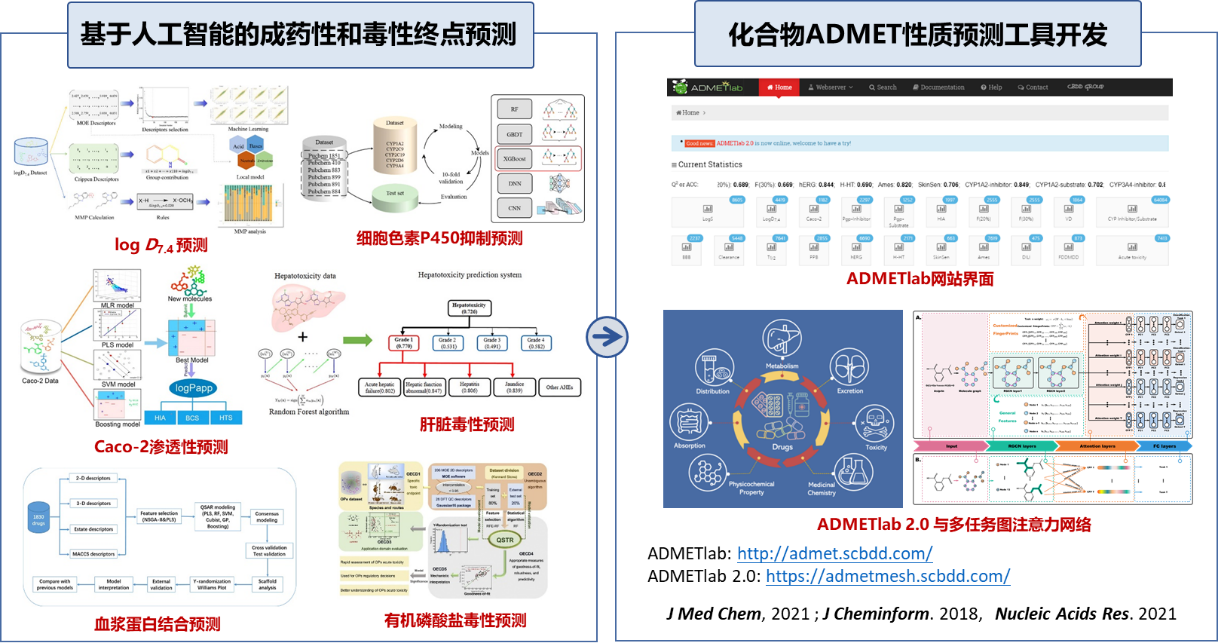
(1)为解决成药性数据缺乏和质量低下的困难问题,我们课题组目前开发了成药性实验数据信息系统(http://admet.scbdd.com/),包含约11万条和29万条总共67个性质终点的化合物基本物理化学性质数据和ADMET数据,是目前国际上已公开发布的数据量最大的成药性信息系统之一。我们将继续利用各种文献挖掘技术和手工校正相结合的方式从文献中提取各种ADMET终点数据,增加ADMET的终点数目和数据量,并进一步优化整合构建高质量的成药性实验数据信息系统。
(2)基于该信息系统中的成药性实验数据,申请人创造性地运用前期开发的化学信息学算法和分子表征技术并结合随机森林、极端梯度提升、深度学习等机器学习技术,发展了口服生物利用度、水溶性、细胞渗透性、logD7.4、P糖蛋白抑制剂、肝毒性等关键ADMET参数的预测模型,大部分所建模型预测精度有效提升10%左右,显著优于国内外文献报导的同类模型。为解决成药性预测的小数据问题,我们利用了迁移学习、多任务学习、自监督、transformer、BERT及图神经网络等新型人工智能技术发展了高精度高效率的药物成药性及毒性预测算法,进一步提升了多个关键ADMET指标预测模型的预测精度。针对一些预测精度差的ADMET性质终点,我们将继续利用新型人工智能技术发展高精度的预测模型来提升这些性质终点的预测精度,从而实现这些ADMET性质终点的精准预测。另外,我们将重点利用多模态+大模型+多任务学习的建模策略进一步发展高精度高效率的成药性预测模型,从而实现ADMET预测模型在药物研发中的实际落地应用。

(3)以上述成药性预测模型为基础,利用多任务图网络深度学习算法开发了关键成药性参数在线计算平台ADMETLab及其更新版本ADMETLab2.0(http://admetmesh.scbdd.com/),可实现17种基本物理化学性质参数、13种药物化学性质参数、24种成药性参数、27种毒性终点及7种警示子结构规则(共597个)的系统性评价,是目前国际上成药性参数评价最多的免费在线计算平台之一。该平台已被辉瑞、诺华、昆明植物所、北京大学医学部和浙江大学等药企和科研院校用于成药性及毒性预测评估,并被写入化学工业出版社出版的《药物设计学》著作中,目前累计访问量达113000余次。作为课题组主要的研究方向之一,我们将继续开发更可靠、更准确的理论预测模型,并构建药物分子ADMET性质预测的软件平台。我们后续将进一步优化整合发展的模型开发功能更加完善的高效高精度的成药性和安全性预测软件平台。

代表性文章:
1:Mining Toxicity Information from Large Amounts of Toxicity Data
2:MG-BERT: leveraging unsupervised atomic representation learning for molecular property prediction
3: ADMETlab 2.0: an integrated online platform for accurate and comprehensive predictions of ADMET properties
4: ADMETlab: a platform for systematic ADMET evaluation based on a comprehensively collected ADMET database
5: ADME properties evaluation in drug discovery: prediction of Caco-2 cell permeability using a combination of NSGA-II and boosting
6: ADMET evaluation in drug discovery. 19. Reliable prediction of human cytochrome P450 inhibition using artificial intelligence approaches
7: Systematic Modeling of log D7.4 Based on Ensemble Machine Learning, Group Contribution, and Matched Molecular Pair Analysis
8: Three-level hepatotoxicity prediction system based on adverse hepatic effects
